¿Buscas optimizar los procesos de tu laboratorio?
Nuestras áreas de trabajo persiguen un mismo objetivo: aportar seguridad y calidad a tu laboratorio con:
¿Cómo quieres mejorar tu laboratorio?
En ICSA llevamos más de 30 años implementando soluciones globales en laboratorios clínicos y de ensayo. Queremos dar con la solución que necesitas. ¿Por dónde empezamos?
Equipos para Anatomía Patológica
Encuentra en nuestros equipos y consumibles la seguridad que estás buscando
Alta tecnología diseñada para garantizar la seguridad a los usuarios, la protección a las muestras y la trazabilidad completa.
- Instrumentos para Anatomía Patológica
- Reactivos para Anatomía Patológica
- Sistemas de control de temperatura
- Instrumentos para Laboratorios Físico-Químicos
- Programas de Mantenimiento para equipos e instrumentos
Consultoría para laboratorios
¿Por qué deberías implementar normas de calidad en tu laboratorio?
- Garantiza la validez técnica de los resultados
- Consigue la trazabilidad completa de todos los procesos de tu laboratorio
- Sé referente en calidad y seguridad
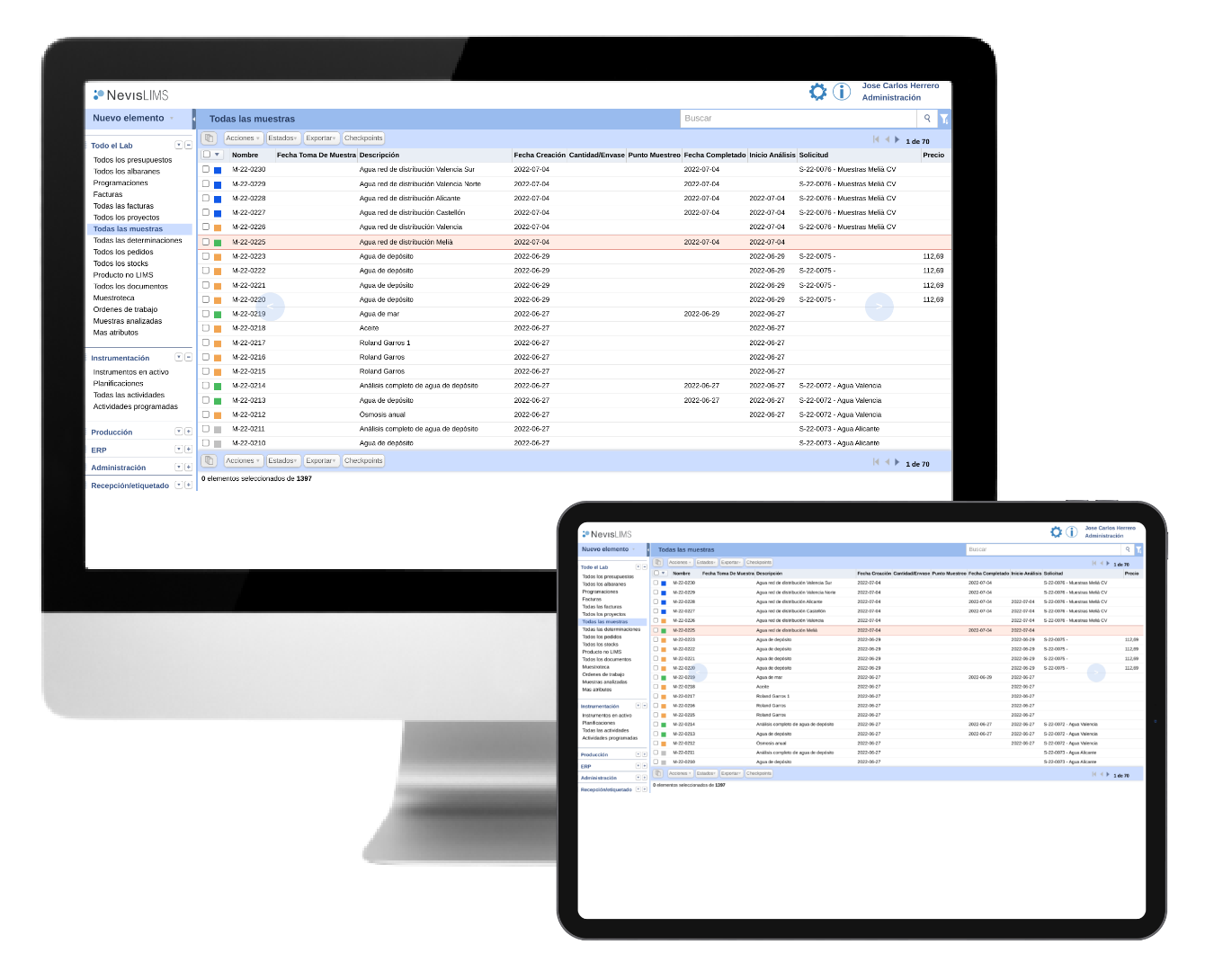
LIMS - Software para laboratorios
Nevis LIMS - Para automatizar todos los procesos de tu laboratorio
- En la nube
- Sin licencias
- Más seguro
- En la nube
- Sin licencias
- Más seguro
- Gestiona las muestras sin errores
- Planifica las rutas de muestreo para optimizar el tiempo de tus analistas
- Garantiza calidad con los módulos específicos basados en ISO 17025
Soluciones tracking
Descubre nuestros sistemas de Identificación por Radiofrecuencia para trazabilidad de muestras
- Localización en tiempo real de tus muestras
- Envío de alertas
- Todo unificado en un mismo software
Más de 500 laboratorios en España disfrutan ya de un espacio más seguro y optimizado

Dra. Ana Calatrava.
Jefa del Servicio de Anatomía Patológica del IVO
“Desde que en el quirófano del IVO envasamos las muestras con atmósfera de protección en el sistema T-FILLER, nuestro laboratorio tiene la garantía de que las piezas llegan en perfecto estado de conservación y refrigeración. Por un lado, hemos conseguido reducir mucho el uso de formol en quirófano. Por otro lado, hemos optimizado la logística, ya que solo se transportan muestras desde quirófano a anatomía patológica una vez al día.”

Cristóbal Sánchez.
CEO de Microgaia Biotech
“El servicio de consultoría de ICSA cumplió todas nuestras expectativas en el proceso de implementación de ISO 17025 en nuestro laboratorio. Necesitábamos una asesoría completa sobre esta norma y nos la dieron. Tras la implantación, hemos ganado confianza en nuestro trabajo, fiabilidad y una mejora en la trazabilidad.”

Rosalía Guerra.
Laboratory Manager de AIMPLAS
“Desde que implantamos Nevis LIMS con todas las funcionalidades personalizadas según nuestros requerimientos, funcionamos de forma mucho más eficiente. ICSA ha sido capaz de escuchar necesidades no típicas de una empresa productiva que atiende actividades, empresas o aplicaciones donde está el plástico.”

Yolanda Pastor.
Responsable de Preanalítica del [Servicio de Análisis Clínicos del] Hospital General de Valencia
“A nosotros Nevis ST2 nos da mucha tranquilidad, ya que estamos seguros de que hemos ido cumpliendo todos nuestros requerimientos establecidos, con unos controles de temperatura y tiempo muy exigentes. Los errores han disminuido considerablemente desde que usamos ST2.”
Casos de éxito

Hospital Universitario Príncipe de Asturias
En el Hospital Príncipe de Asturias de Madrid, el Dr. Busteros, Jefe de Servicio en el área de Anatomía Patológica, destaca el notable éxito de la implementación del sistema de trazabilidad FINA. Antes de incorporar esta tecnología, el proceso de gestión de bloques se realizaba manualmente, demandando 5 horas semanales y la dedicación exclusiva de dos técnicos.

Hospital General de Granollers
La Dra. Inma Méndez, Jefa del Servicio de Anatomía Patológica del Hospital de Granollers, nos cuenta su experiencia con los sistemas de trazabilidad Dreampath.

Hospital Universitario La Paz
El Hospital Universitario La Paz archiva 600 bloques diarios con el sistema de trazabilidad para archivo de bloques FINA
¿Conoces nuestros Eventos?
Envasado de biopsias sin formol y rastreabilidad desde quirófano hasta AP
Descubre la mejor combinación para garantizar la seguridad del paciente, de la biopsia y del operario: T-FILLER + NEVIS TRACK
3 de mayo 2024
12:00 h. *Hora peninsular y Baleares.
Descubre la mejor combinación para garantizar la seguridad del paciente, de la biopsia y del operario: T-FILLER + NEVIS TRACK

Gestión de datos y trazabilidad en la cadena de producción farmacéutica con Nevis LIMS
Garantiza la trazabilidad de las muestras y resultados facilitando el cumplimiento de las GMP
24 de mayo de 2024
11:00 h. *Hora peninsular y Baleares.
Garantiza la trazabilidad de las muestras y resultados facilitando el cumplimiento de las GMP

¿Cuál es el rol de LIMS en el cumplimiento de ISO/IEC 17025?
Webinar
3 de mayo 2024
11:00 h. *Hora peninsular y Baleares.
¿Cuál es el rol de LIMS en el cumplimiento de ISO/IEC 17025?

LIMS O ELN ¿Cuál es mejor para mi laboratorio?
Descubre las principales características de un LIMS y un ELN y los diferentes beneficios que te pueden aportar uno u otro
19 de abril de 2024
11:00 h. *Hora peninsular y Baleares.
Descubre las principales características de un LIMS y un ELN y los diferentes beneficios que te pueden aportar uno u otro.

Control de temperatura y tracking de muestras en Análisis Clínicos
Webinar
21 de junio de 2024
11:00 h. *Hora peninsular y Baleares.
Descubre el sistema que controla la temperatura de las muestras en todo el proceso preanalítico, así como su geolocalización desde el punto de extracción hasta su llegada al laboratorio de Análisis Clínicos.








